開(kāi)封正規(guī)外泌體提取試劑供應(yīng)商
- 產(chǎn)地
- 蘇州
- 品牌
- 外泌體提取試劑
- 型號(hào)
- 齊全
- 是否定制
- 是
外泌體是細(xì)胞間進(jìn)行物質(zhì)運(yùn)輸和信息交流的重要工具,可以通過(guò)調(diào)節(jié)免疫功能促進(jìn)一些病癥的增殖,血管新生和一些病癥轉(zhuǎn)移。與細(xì)菌傳染,幫助細(xì)菌逃避免疫關(guān)系很大,并與心血管疾病,老年癡呆等疾病具有密切關(guān)系。外泌體可通過(guò)流式、WB(檢測(cè)指標(biāo)有CD9,CD63,CD81)、電鏡觀察、NTA粒徑追蹤等手段檢測(cè),普遍應(yīng)用于藥物載體、疾病診斷marker、精細(xì)醫(yī)療、一些病癥治病等方面研究。由于外泌體直徑小,樣本含量低,提取十分困難。已有的外泌體分離方式有密度梯度離心、超濾離心法、免疫磁珠抗體捕獲、商用試劑盒等。但到目前為止,仍沒(méi)有一種提取方法能同時(shí)保證外泌體的含量、純度以及生物活性。外泌體提取:基于聚合物的沉淀技術(shù)。開(kāi)封正規(guī)外泌體提取試劑供應(yīng)商

外泌體相關(guān)蛋白質(zhì)與肺病的診斷:近年來(lái)眾多文獻(xiàn)報(bào)道,肺病細(xì)胞分泌的外泌體中富含多種蛋白質(zhì)并促進(jìn)肺病的發(fā)生的發(fā)展,是早期診斷肺病的有效途徑。有研究發(fā)現(xiàn),NSCLC患者肺組織外泌體表面EGFR免疫染色呈陽(yáng)性的占80%,而慢性肺炎組織的外泌體EGFR呈陽(yáng)性的只占2%,因而認(rèn)為外泌體的EGFR蛋白可以用作NSCLC與慢性肺炎鑒別診斷的生物標(biāo)志物。Park等通過(guò)Sys-BodyFlu-id數(shù)據(jù)庫(kù)分析發(fā)現(xiàn)153種特異性胸腔積液外泌體蛋白質(zhì),進(jìn)一步的Westernblotting分析顯示多種特異性胸腔積液外泌體蛋白參與EGFR信號(hào)傳導(dǎo)途徑以促進(jìn)一些病癥的發(fā)生的發(fā)展,因此外泌體蛋白可能作為肺病診斷篩查的生物學(xué)標(biāo)記物。近幾年來(lái),市場(chǎng)上已出現(xiàn)各種商業(yè)化的外泌體提取試劑盒。開(kāi)封正規(guī)外泌體提取試劑供應(yīng)商外泌體提取:超離法是較常用的外泌體純化手段,采用低速離心、高速離心交替進(jìn)行。

研究表明被特定部位的細(xì)胞獲取的一些病癥外泌體可為一些病癥的轉(zhuǎn)移準(zhǔn)備轉(zhuǎn)移前微環(huán)境。用肺轉(zhuǎn)傾向的一些病癥細(xì)胞來(lái)源的外泌體處理小鼠后可使骨轉(zhuǎn)傾向的一些病癥細(xì)胞重新定向。外泌體的蛋白質(zhì)組學(xué)分析發(fā)現(xiàn)不同部位傾向性的一些病癥細(xì)胞來(lái)源的外泌體具有不同的整合素(integrin)表達(dá)譜,整合素α6β4和α6β1與肺轉(zhuǎn)有關(guān),而整合素αvβ5與肝轉(zhuǎn)有關(guān)。敲低整合素α6β4和αvβ5可減少外泌體被靶部位細(xì)胞獲取,進(jìn)而分別降低了肺和肝的轉(zhuǎn)移。進(jìn)一步研究發(fā)現(xiàn)外泌體整合素被細(xì)胞獲取后啟動(dòng)了Src的磷酸化和促炎的S100基因的表達(dá)。較后通過(guò)臨床數(shù)據(jù)分析顯示外泌體整合素可作為預(yù)測(cè)一些病癥轉(zhuǎn)移的部位傾向性的診斷指標(biāo)。
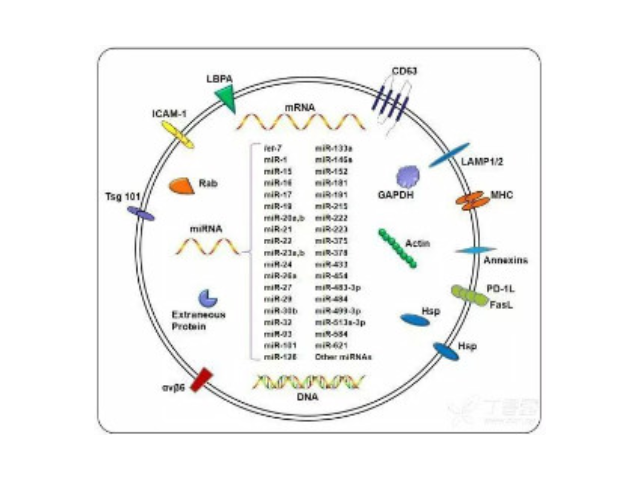
人體內(nèi)多種細(xì)胞及體液均可分泌外泌體,包括內(nèi)皮細(xì)胞、免疫細(xì)胞、血小板、平滑肌細(xì)胞等。當(dāng)其由宿主細(xì)胞被分泌到受體細(xì)胞中時(shí),外泌體可通過(guò)其攜帶的蛋白質(zhì)、核酸、脂類等來(lái)調(diào)節(jié)受體細(xì)胞的生物學(xué)活性。外泌體介導(dǎo)的細(xì)胞間通訊主要通過(guò)以下三種方式:一是外泌體膜蛋白可以與靶細(xì)胞膜蛋白結(jié)合,進(jìn)而靶細(xì)胞細(xì)胞內(nèi)的信號(hào)通路。二是在細(xì)胞外基質(zhì)中,外泌體膜蛋白可以被蛋白酶剪切,剪切的碎片可以作為配體與細(xì)胞膜上的受體結(jié)合,從而細(xì)胞內(nèi)的信號(hào)通路。有報(bào)道稱一些外泌體膜上蛋白在其來(lái)源細(xì)胞膜上未能檢測(cè)出。近幾年來(lái),市場(chǎng)上已出現(xiàn)各種商業(yè)化的外泌體提取試劑盒。

由于這些核酸被囊膜包裹而被保護(hù),穩(wěn)定性高,不易降解,是一種用于一些病癥診斷和預(yù)后監(jiān)測(cè)的非常理想的新型生物標(biāo)記物一些疾病的早期診斷、用藥監(jiān)控、預(yù)后判斷。近年來(lái),隨著人們對(duì)外泌體的研究和認(rèn)識(shí)加深,外泌體檢測(cè)作為一種新型的液體活檢熱點(diǎn)技術(shù)已被許多臨床科研機(jī)構(gòu)普遍地應(yīng)用于一些病癥和疾病的無(wú)創(chuàng)診斷、治病和監(jiān)測(cè);如何高效地提取外泌體是實(shí)現(xiàn)這項(xiàng)新興液體活檢技術(shù)臨床常規(guī)化應(yīng)用的關(guān)鍵。外泌體(Exosome)是從體液(尿液、血液、唾液、腹水、胸腹水等)和細(xì)胞液中快速提取的,其是活細(xì)胞分泌到胞外的囊泡樣小體,含有多種蛋白和核酸分子(DNA、RNA、以及miRNA),在體內(nèi)細(xì)胞間物質(zhì)和信號(hào)轉(zhuǎn)導(dǎo)中起到重要作用。用于外泌體提取的體液收集注意事項(xiàng):操作要輕柔迅速。長(zhǎng)沙正規(guī)外泌體提取試劑進(jìn)貨價(jià)
外泌體提取:較常見(jiàn)的過(guò)濾膜具有0.8μm、0.45μm或0.22μm的孔徑。開(kāi)封正規(guī)外泌體提取試劑供應(yīng)商
1983年,外泌體初次于綿羊網(wǎng)織紅細(xì)胞中被發(fā)現(xiàn),1987年Johnstone將其命名為“exosome”。多種細(xì)胞在正常及病理狀態(tài)下均可分泌外泌體。其主要來(lái)源于細(xì)胞內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,經(jīng)多囊泡體外膜與細(xì)胞膜融合后釋放到胞外基質(zhì)中。所有培養(yǎng)的細(xì)胞類型均可分泌外泌體,且外泌體天然存在于體液中,包括血液、唾液、尿液、腦脊液和乳汁中。有關(guān)他們分泌和攝取及其組成、“運(yùn)載物”和相應(yīng)功能的精確分子機(jī)制剛剛開(kāi)始研究。外泌體目前被視為特異性分泌的膜泡,參與細(xì)胞間通訊,對(duì)外泌體的研究興趣日益增長(zhǎng),無(wú)論是研究其功能還是了解如何將其用于微創(chuàng)診斷的開(kāi)發(fā)。開(kāi)封正規(guī)外泌體提取試劑供應(yīng)商
作為一種分子通斷開(kāi)關(guān)的KRAS發(fā)生突變時(shí)會(huì)處于“開(kāi)啟”狀態(tài)。在80%~95%的胰腺導(dǎo)管腺病(PDAC)當(dāng)中,這個(gè)基因發(fā)生突變,這也是這種一些疾病中較為常見(jiàn)的突變。這些研究人員證實(shí)iExosome能夠運(yùn)送特異性地靶向KRAS的siRNA和shRNA分子,并且比他們的合成對(duì)應(yīng)物脂質(zhì)體(liposome)更加高效。脂質(zhì)體不具有外泌體表現(xiàn)出的天然復(fù)雜性和優(yōu)勢(shì)。德州大學(xué)MD安德森一些疾病中心一些疾病生物學(xué)助理教授ValerieLeBleu博士說(shuō),“我們的研究提示著與脂質(zhì)體相比,外泌體表現(xiàn)出運(yùn)送siRNA分子和壓制侵襲性胰腺瘤生長(zhǎng)的優(yōu)異能力。我們也證實(shí)外泌體表面上的CD47存在允許它們躲避來(lái)自循環(huán)單核細(xì)胞...
- 徐州外泌體提取試劑單價(jià) 2025-07-15
- 武漢正規(guī)外泌體提取試劑廠家 2025-07-15
- 鄭州正規(guī)外泌體提取試劑哪家便宜 2025-07-15
- 貴陽(yáng)外泌體提取試劑哪里買 2025-07-15
- 廣州正規(guī)外泌體提取試劑產(chǎn)品介紹 2025-07-15
- 南京外泌體提取試劑單價(jià) 2025-07-14
- 唐山外泌體提取試劑供應(yīng)商 2025-07-14
- 南昌正規(guī)外泌體提取試劑廠家 2025-07-14
- 寧波外泌體提取試劑廠家直銷 2025-07-14
- 武漢正規(guī)外泌體提取試劑哪里買 2025-07-14
- 成都正規(guī)外泌體提取試劑廠家現(xiàn)貨 2025-07-14
- 北京外泌體提取試劑供應(yīng)商 2025-07-14
- 重慶正規(guī)外泌體提取試劑生產(chǎn)廠家 2025-07-14
- 長(zhǎng)沙外泌體提取試劑產(chǎn)品介紹 2025-07-14
- 貴陽(yáng)外泌體提取試劑產(chǎn)品介紹 2025-07-13
- 珠海外泌體提取試劑哪家便宜 2025-07-13


- 南昌正規(guī)細(xì)胞外基質(zhì)膠廠家推薦 07-15
- 武漢正規(guī)外泌體提取試劑廠家 07-15
- 開(kāi)封細(xì)胞外基質(zhì)膠價(jià)格 07-15
- 鄭州正規(guī)外泌體提取試劑哪家便宜 07-15
- 貴陽(yáng)外泌體提取試劑哪里買 07-15
- 唐山細(xì)胞外基質(zhì)膠單價(jià) 07-15
- 溫州唐山細(xì)胞外基質(zhì)膠 07-15
- 廣州正規(guī)外泌體提取試劑產(chǎn)品介紹 07-15
- 南京外泌體提取試劑單價(jià) 07-14
- 唐山外泌體提取試劑供應(yīng)商 07-14