- 產地
- 蘇州
- 品牌
- 外泌體提取試劑
- 型號
- 齊全
- 是否定制
- 是
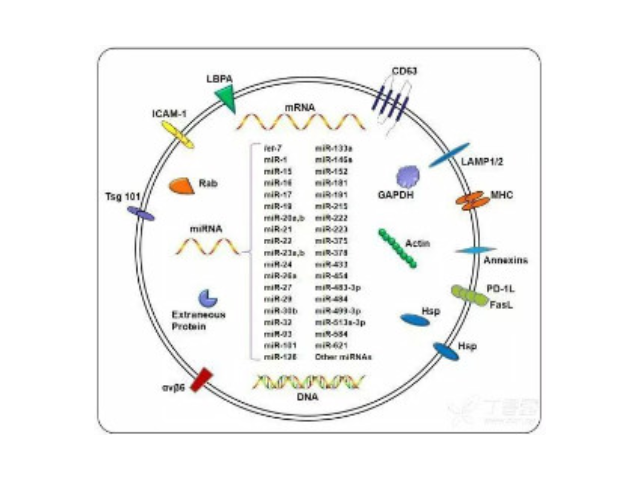
1983年,外泌體初次于綿羊網織紅細胞中被發現,1987年Johnstone將其命名為“exosome”。多種細胞在正常及病理狀態下均可分泌外泌體。其主要來源于細胞內溶酶體微粒內陷形成的多囊泡體,經多囊泡體外膜與細胞膜融合后釋放到胞外基質中。所有培養的細胞類型均可分泌外泌體,且外泌體天然存在于體液中,包括血液、唾液、尿液、腦脊液和乳汁中。有關他們分泌和攝取及其組成、“運載物”和相應功能的精確分子機制剛剛開始研究。外泌體目前被視為特異性分泌的膜泡,參與細胞間通訊,對外泌體的研究興趣日益增長,無論是研究其功能還是了解如何將其用于微創診斷的開發。如何高效地提取外泌體是實現這項新興液體活檢技術臨床常規化應用的關鍵如純度和回收率低,雜蛋白較多(假陽性),顆粒大小不均一,產生難以去除的聚合物。唐山外泌體提取試劑報價
為了分離外泌體,研究人員用兩個這樣的單元串聯構建了一個裝置。首先,使用聲波從血液樣品中除去細胞和血小板。一旦細胞和血小板被去除,樣品進入第二個微流體單元,然后使用較高頻率的聲波將外泌體與稍大的細胞外囊泡分開。這項工作的通訊作者之一,麻省理工學院材料科學與工程系科學家MingDao博士說:“聲波更溫和。而且在分離時,這些囊泡受處理的時間只有1秒鐘或更短。這是一個很大的優勢。”使用該設備,處理100微升未稀釋血液樣本只需要不到25分鐘。“這種新技術可以解決當前外泌體分離技術的缺點,如周期長,一致性差,產量低,污染以及完整性受損等。我們想要把提取高質量的外泌體的過程簡化為按一個按鈕就在10分鐘內獲得所需樣品一樣簡單。”研究人員們說。蕪湖正規外泌體提取試劑報價有的是通過特殊設計的過濾器過濾掉雜質成分,有的則采用空間排阻色譜法(SEC)進行分離純化。

外泌體的提取方法:1、磁珠免疫法。外泌體表面有其特異性標記物(如CD63、CD9蛋白),用包被抗標記物抗體的磁珠與外泌體囊泡孵育后結合,即可將外泌體吸附并分離出來。磁珠法具有特異性高、操作簡便、不影響外泌體形態完整等優點,但是效率低,外泌體生物活性易受pH和鹽濃度影響,不利于下游實驗,難以普遍普及。2、多聚物沉淀法。聚乙二醇(PEG)為常用的多聚物,可與疏水性蛋白和脂質分子結合共沉淀,早先應用于從血清等樣本中收集病毒,現在也被用來沉淀外泌體,其原理可能與競爭性結合游離水分子有關。利用PEG沉淀外泌體存在不少問題:比如純度和回收率低,雜蛋白較多(假陽性),顆粒大小不均一,產生難以去除的聚合物,機械力或者吐溫-20等化學添加物將會破壞外泌體等
外泌體提取:尺寸排阻色譜。尺寸排阻色譜(Size-exclusionchromatography,SEC)是基于大小而非分子量實現分離大分子。該技術應用填充多孔聚合物微球的柱子,分子根據其直徑通過微球,半徑小的分子需要更長的時間才能通過色譜柱的孔隙遷移,而大分子則從色譜柱中更早地洗脫。尺寸排阻色譜可以精確分離大小分子。此外,可以將不同的洗脫溶液應用于該方法。與離心方法相比,色譜分離已被證明具有更多優勢,因為通過色譜分離的外泌體不受剪切力的影響,這可能會改變囊泡的結構。目前,SEC是一種普遍接受的分離血液和尿液中外泌體的技術。不過,該方法耗時較長,不適合大量樣本處理由于外泌體的特殊結構和功能,使得它具有潛在的應用價值。
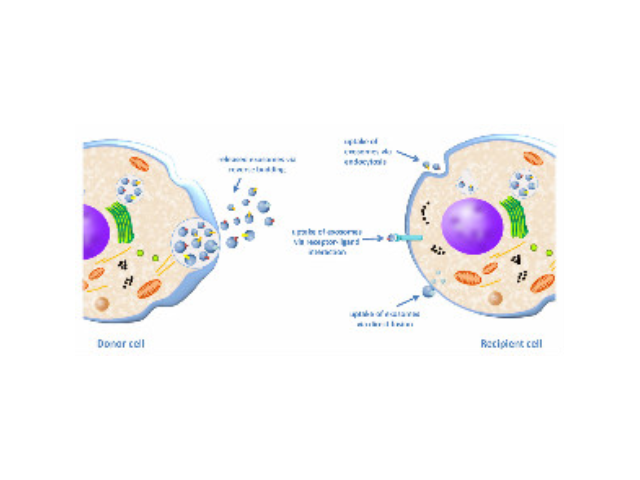
外泌體的提取方法:1.超速離心法(差速離心)。超離法是較常用的外泌體純化手段,采用低速離心、高速離心交替進行,可分離到大小相近的囊泡顆粒。超離法因操作簡單,獲得的囊泡數量較多而廣受歡迎,但過程比較費時,且回收率不穩定(可能與轉子類型有關),純度也受到質疑;此外,重復離心操作還有可能對囊泡造成損害,從而降低其質量。2.密度梯度離心。在超速離心力作用下,使蔗糖溶液形成從低到高連續分布的密度階層,是一種區帶分離法。通過密度梯度離心,樣品中的外泌體將在1.13-1.19g/ml的密度范圍富集。此法獲得的外泌體純度較高,但步驟繁瑣,耗時,對離心時間極為敏感外泌體:形成了一種全新的細胞間信息傳遞系統,影響細胞的生理狀態并與多種疾病的發生與進程密切相關。廈門外泌體提取試劑報價
首先在無菌條件下提取人體體液,并用PBS緩沖液進行稀釋。唐山外泌體提取試劑報價
外泌體研究的主要應用:外泌體的功能取決于其所來源的細胞類型,其可參與到機體免疫應答、抗原提呈、細胞遷移、細胞分化、一些病癥侵襲等方方面面。有研究表明一些病癥來源的外泌體參與到一些病癥細胞與基底細胞的遺傳信息的交換,從而導致大量新生血管的生成,促進了一些病癥的生長與侵襲。一些病癥。一些病癥轉移。來自白血病干細胞的外泌體促進急性骨髓性白血病(AML)細胞的增殖、遷移和壓制細胞凋亡。治病靶標。利用外泌體遞送小干擾RNA來沉默KRASG12D,從而特異性高效靶向至胰腺病細胞,以明顯降低RAS活化、病細胞增殖和轉移過程。免疫。β細胞將含有蛋白質和miRNA的外泌體釋放到細胞外,并可轉移到其他代謝部位或免疫內皮細胞,有利于維持葡萄糖體內平衡或造成胰島素抵抗。心血管。外泌體介導miR-155從平滑肌細胞轉移到內皮細胞導致了內皮細胞的損傷促進動脈硬化。分子標記。疾病診斷。在酒精性肝病、NASH、菌類性肝炎、藥物性肝損傷和肝細胞病中發現循環EVs的水平上升。預后標志。唐山外泌體提取試劑報價
作為一種分子通斷開關的KRAS發生突變時會處于“開啟”狀態。在80%~95%的胰腺導管腺病(PDAC)當中,這個基因發生突變,這也是這種一些疾病中較為常見的突變。這些研究人員證實iExosome能夠運送特異性地靶向KRAS的siRNA和shRNA分子,并且比他們的合成對應物脂質體(liposome)更加高效。脂質體不具有外泌體表現出的天然復雜性和優勢。德州大學MD安德森一些疾病中心一些疾病生物學助理教授ValerieLeBleu博士說,“我們的研究提示著與脂質體相比,外泌體表現出運送siRNA分子和壓制侵襲性胰腺瘤生長的優異能力。我們也證實外泌體表面上的CD47存在允許它們躲避來自循環單核細胞...
- 徐州外泌體提取試劑單價 2025-07-15
- 武漢正規外泌體提取試劑廠家 2025-07-15
- 鄭州正規外泌體提取試劑哪家便宜 2025-07-15
- 貴陽外泌體提取試劑哪里買 2025-07-15
- 廣州正規外泌體提取試劑產品介紹 2025-07-15
- 南京外泌體提取試劑單價 2025-07-14
- 唐山外泌體提取試劑供應商 2025-07-14
- 南昌正規外泌體提取試劑廠家 2025-07-14
- 寧波外泌體提取試劑廠家直銷 2025-07-14
- 武漢正規外泌體提取試劑哪里買 2025-07-14
- 成都正規外泌體提取試劑廠家現貨 2025-07-14
- 北京外泌體提取試劑供應商 2025-07-14
- 重慶正規外泌體提取試劑生產廠家 2025-07-14
- 長沙外泌體提取試劑產品介紹 2025-07-14
- 貴陽外泌體提取試劑產品介紹 2025-07-13
- 珠海外泌體提取試劑哪家便宜 2025-07-13


- 開封正規無血清細胞凍存液平均價格 07-16
- 太原無血清細胞凍存液服務電話 07-16
- 正規無血清細胞凍存液單價 07-16
- 正規外泌體提取試劑哪家好 07-15
- 廣州正規無血清細胞凍存液直銷廠家 07-15
- 金華細胞外基質膠廠家直銷 07-15
- 徐州外泌體提取試劑單價 07-15
- 北京無血清細胞凍存液單價 07-15
- 蘇州正規細胞外基質膠廠家直銷 07-15
- 寧波成都細胞外基質膠 07-15






