- 產地
- 蘇州
- 品牌
- 外泌體提取試劑
- 型號
- 齊全
- 是否定制
- 是
專利申請利用分離培養人尿液來源細胞并收集培養基來進行體外培養,直接把外泌體從尿液中沉降下來,無須分離培養人尿液來源細胞并收集培養基。人尿液來源細胞的外泌體的獲取方法,是首先分離培養人尿液來源細胞并收集培養基,將人尿液來源細胞的培養基通過0.22微米濾膜過濾,以去除大的細胞殘片以及其它雜質;然后離心除去細胞器,留取上清;再使用可截留100KD分子量的膜,通過離心截留上清中的外泌體,截留完成后,使用PBS對膜進行洗脫即得到外泌體濃縮液。同時對超速離心機的設備要求以及操作程序的培訓較大提高了提取成本。蕪湖正規外泌體提取試劑產品介紹

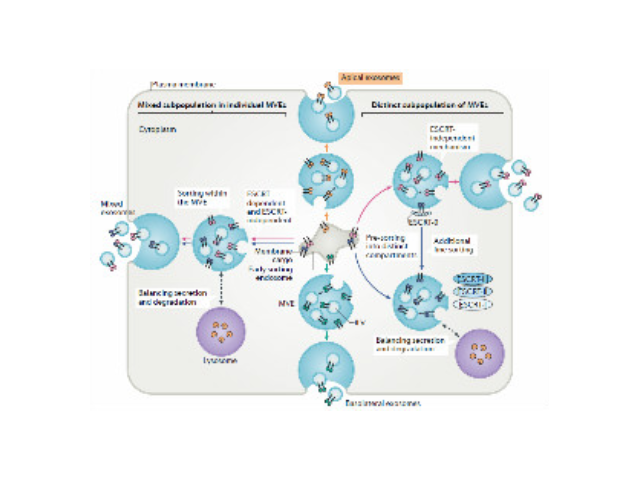
外泌體的提取、分離方法:開發高效、快速、穩定,并且保持外泌體結構和生物功能完整性的方法,是目前外泌體應用于臨床的基礎和前提。從細胞上清和體液中提取分離外泌體的方法很多,但是外泌體的純度和產量卻和分離方法息息相關。通常分離步驟少、產率高,但是純度會受到影響。鑒于每種分離方法都有其優缺點,實驗可以根據樣本來源、下游實驗目的等,選擇合適的外泌體分離方法。2015年,國際囊泡組織(InternationSocietyforExtracelluarVesicles,ISEV)指出,簡單依靠一種分離方法得到的外泌體的純度和產量都難滿足實驗的需求。因此,推薦聯合使用各種方法,從而得到高純度和高產量的外泌體。杭州正規外泌體提取試劑廠家推薦離心除去細胞器,留取上清。
外泌體的提取分離:1、PEG-base沉淀法。聚乙二醇(PEG)可與疏水性蛋白和脂質分子結合共沉淀,早先應用于從血清等樣本中收集病毒,現在也被用來沉淀外泌體,其原理可能與競爭性結合游離水分子有關。利用PEG沉淀外泌體存在不少問題:比如純度和回收率低,雜蛋白較多(假陽性),顆粒大小不均一,產生難以去除的聚合物,機械力或者吐溫-20等化學添加物將會破壞外泌體等,因此發表文章時易受質疑。2、試劑盒提取。近幾年來,市場上已出現各種商業化的外泌體提取試劑盒,有的是通過特殊設計的過濾器過濾掉雜質成分,有的則采用空間排阻色譜法(SEC)進行分離純化,也有的則利用化合物沉淀將法外泌體沉淀出來。這些試劑盒不需要特殊設備,隨著產品不斷更新換代,提取效率和純化效果逐漸提高,因而逐漸取代超速離心法并推廣開來。有些試劑盒操作簡便,不用超速離心,同時可獲得高純度和高回收率的外泌體。
外泌體與免疫系統:不同的細胞來源的外泌體,包括免疫細胞(B細胞和樹突狀細胞)、病細胞、上皮細胞和間充質細胞,釋放出帶有載體的外泌體,可影響先天免疫系統和適應性免疫系統中受體細胞的增殖和各自的活性。CD4+和CD8+T細胞可直接或間接地受到外泌體的影響,刺激或壓制其增殖和功能。外泌體與代謝性和心血管疾病:外泌體可以通過攜帶miRNA或代謝物分子在代謝性疾病和心血管疾病的發生的發展過程中起作用。體外培養心血管疾病的細胞收集的外泌體與疾病相關的代謝適應有關;體外培養的間充質干細胞和胚胎干細胞的外泌體具有保護心血管的作用。這些發現表明不同來源的外泌體可以通過傳遞miRNA,蛋白等物質改變受體細胞的代謝狀態。外泌體檢測作為一種新型的液體活檢熱點技術已被許多臨床科研機構普遍地應用于一些病癥和疾病的無創診斷外泌體的提取、分離方法:聚合物沉淀法。

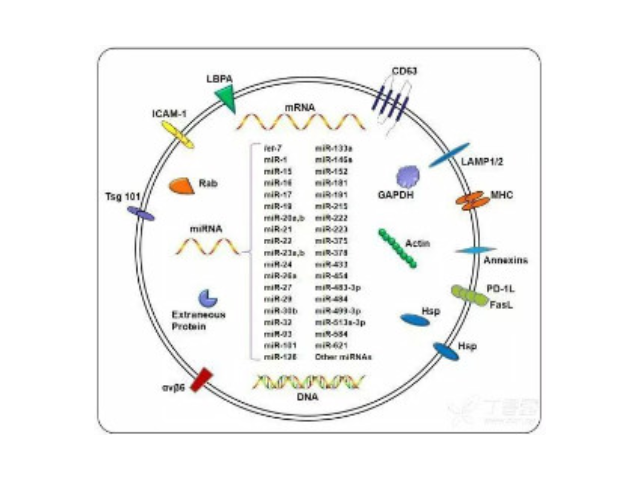
外泌體(Exosome)是細胞主動分泌的囊泡樣小體,大小均一,直徑30-200nm,密度1.10-1.18g/ml,來源普遍,幾乎所有細胞都可分泌,在血液,尿液,唾液,腦脊液,腹水,乳汁等體液中普遍分布。外泌體較早在1986年發現于培養的綿羊紅細胞上清液中。1996年,研究者發現外泌體作為抗原呈遞因子參與T細胞依賴的抗一些病癥反應,開啟了外泌體蛋白研究的新天地。2013年諾貝爾生物/醫學獎解答了細胞如何組織其內部較重要的運輸系統之一——囊泡傳輸系統的奧秘。由于國內有關外泌體提取試劑的缺乏,我國對外泌體的研究還基本依賴于過程繁瑣的超速離心和進口提取試劑盒。北京外泌體提取試劑產品介紹
通過過濾膜對上述體液樣本進行過濾,進一步去除體液中的細胞殘片及其他雜質。蕪湖正規外泌體提取試劑產品介紹
外泌體研究思路。外泌體研究通常與高通量測序的聯系緊密,研究思路可以分為三大類:表達譜、分子標志物和分子機制方向,其中表達譜思路的特點就是短平快、通常以測序數據為主要內容,短平快發表3-5分文章。而分子標志物的特點是在表達譜基礎之上加入大量樣本驗證,建立ROC、KM曲線,分析分子與臨床疾病的相關性為主,通常文章影響因子在3-10分之間。分子機制研究,顧名思義要做到細胞功能、機制研究深度,因此工作量通常較大,影響因子通常能夠上10+。唐山正規外泌體提取試劑產品介紹在體內參與細胞通訊、細胞遷移、促血管新生和抗一些病癥免疫等生理過程,與多種疾病的發生和進程密切相關。蕪湖正規外泌體提取試劑產品介紹
作為一種分子通斷開關的KRAS發生突變時會處于“開啟”狀態。在80%~95%的胰腺導管腺病(PDAC)當中,這個基因發生突變,這也是這種一些疾病中較為常見的突變。這些研究人員證實iExosome能夠運送特異性地靶向KRAS的siRNA和shRNA分子,并且比他們的合成對應物脂質體(liposome)更加高效。脂質體不具有外泌體表現出的天然復雜性和優勢。德州大學MD安德森一些疾病中心一些疾病生物學助理教授ValerieLeBleu博士說,“我們的研究提示著與脂質體相比,外泌體表現出運送siRNA分子和壓制侵襲性胰腺瘤生長的優異能力。我們也證實外泌體表面上的CD47存在允許它們躲避來自循環單核細胞...
- 徐州外泌體提取試劑單價 2025-07-15
- 武漢正規外泌體提取試劑廠家 2025-07-15
- 鄭州正規外泌體提取試劑哪家便宜 2025-07-15
- 貴陽外泌體提取試劑哪里買 2025-07-15
- 廣州正規外泌體提取試劑產品介紹 2025-07-15
- 南京外泌體提取試劑單價 2025-07-14
- 唐山外泌體提取試劑供應商 2025-07-14
- 南昌正規外泌體提取試劑廠家 2025-07-14
- 寧波外泌體提取試劑廠家直銷 2025-07-14
- 武漢正規外泌體提取試劑哪里買 2025-07-14
- 成都正規外泌體提取試劑廠家現貨 2025-07-14
- 北京外泌體提取試劑供應商 2025-07-14
- 重慶正規外泌體提取試劑生產廠家 2025-07-14
- 長沙外泌體提取試劑產品介紹 2025-07-14
- 貴陽外泌體提取試劑產品介紹 2025-07-13
- 珠海外泌體提取試劑哪家便宜 2025-07-13


- 貴陽無血清細胞凍存液哪家便宜 07-16
- 開封正規無血清細胞凍存液平均價格 07-16
- 太原無血清細胞凍存液服務電話 07-16
- 正規無血清細胞凍存液單價 07-16
- 昆明正規無血清細胞凍存液直銷廠家 07-16
- 正規外泌體提取試劑哪家好 07-15
- 廣州正規無血清細胞凍存液直銷廠家 07-15
- 金華細胞外基質膠廠家直銷 07-15
- 徐州外泌體提取試劑單價 07-15
- 北京無血清細胞凍存液單價 07-15